中心原子为sp2杂化的V形分子有哪些
说到V形分子,咱们首先得知道它们通常是三原子组成的分子,而且中心原子得带上一对孤对电子才行。简单来说:
- 中心原子上有孤对电子时,三原子分子往往呈现V形构型。
- 当中心原子不仅和两个原子成键,还带有一对孤对电子时,这个中心原子一般是sp2杂化。
举个经典例子,SO2分子里,S原子的价层电子数计算是 (6-2*2)/2=1对孤对电子,所以它是V形,中心原子是sp2杂化。再根据等电子体原理,价电子数一样的分子构型也一样,比如O3和SO2就是同样的V形结构。类似的分子还有SeO2、NO2等等,都是中心原子sp2杂化且呈V形的分子。
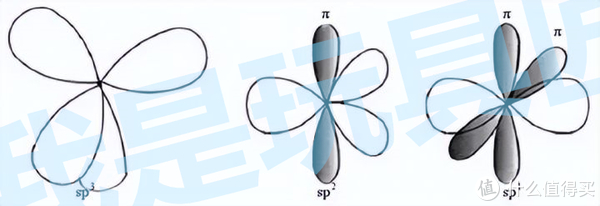
S原子的杂化轨道方式为什么以及如何判断
咱们来聊聊S原子的杂化轨道哈,特别是像S8这种分子里:
- S8分子结构显示,每个S原子成键电子对数是2,孤电子对数也是2,所以价层电子对总共是4对。
- 这就意味着S原子采用的杂化方式是sp3杂化,这也是S8稳定存在的原因。
除此之外,咱们还能看到同周期元素的性质变化,比如Mg和Al的第一电离能是Al>Mg,电负性顺序是F>O等等,虽然有点扯远,但这些性质对理解杂化和分子性质也挺有帮助的。
判断杂化类型其实不难,只要搞清楚成键电子对和孤对电子对的数量,然后根据VSEPR理论,搭配杂化轨道理论,就能轻松判断。比如S8就是sp3,SO2是sp2,这样对照着理解,超实用!

相关问题解答
-
什么是V形分子,为什么中心原子带孤对电子?
哎呀,V形分子其实就是分子形状像字母“V”,通常中心原子和两个原子成键,但还带着一对孤对电子。这个孤对电子可不是摆设,它们会占据空间,导致分子弯曲,所以形状就成了V形啦,像SO2、O3都是典型例子,超级有趣! -
为什么SO2的中心原子是sp2杂化?
呃,这个嘛,SO2的S原子不仅和两个氧原子成键,还带有一对孤对电子。根据杂化轨道理论,这样的电子排布最稳定的是sp2杂化,能让分子形成平面三角形的V形结构。说白了,就是这样杂化最舒服,分子最稳当啦! -
S8分子的S原子杂化类型是怎么判断的?
嘿嘿,判断S8里S原子杂化类型其实挺简单。你数数它的成键电子对和孤对电子对,都是2对,加起来4对电子对就是典型的sp3杂化啦。这种杂化方式让S8形成环状结构,非常稳定,真是大自然的巧妙设计! -
等电子体原理在判断分子构型中起什么作用?
额,这个等电子体原理就是说,如果几个分子的价电子数一样,那么它们的分子构型也差不多。比如SO2和O3,它们电子数一样,所以都呈V形。这原则超方便,帮我们快速预测分子形状,真是太实用了,别忘了哦!

发布评论